適正使用ガイド
注意すべき副作用とその対策
肝機能異常
肝機能異常の発現状況
- イムセラ投与中に肝機能検査値異常(ALT、AST、γ-GTP等の上昇)が現れることがあります。
- 本剤の国内臨床試験における肝機能検査値異常の発現率は31.1%(50/161例)でした。なお、「肝胆道系障害」に分類される副作用は報告されていません。
- 発現例の多くは本剤投与開始後3~4ヵ月以内に認められていますが、その後も認められることがあります。
- 国内臨床試験において、ALT、ASTの平均値は、イムセラ群では投与開始15日後には上昇がみられ、投与開始3ヵ月後に最も高値を示し、その後は一定に推移しました(図)。なお、投与を中止した症例では、ALTおよびASTの上昇は投与中止3ヵ月後までには基準値範囲内まで回復しました。
- γ-GTPの平均値は、イムセラ群では投与開始15日後には上昇がみられ、投与開始6ヵ月後に最も高値を示しました(図)
- 国内第Ⅱ相試験において、肝機能検査値の基準に合致した後に投与を中止した症例は、イムセラ0.5mg群とプラセボ群では同程度でした(表)。
図 6ヵ月間の肝酵素の変化量推移〔国内第Ⅱ相試験〕
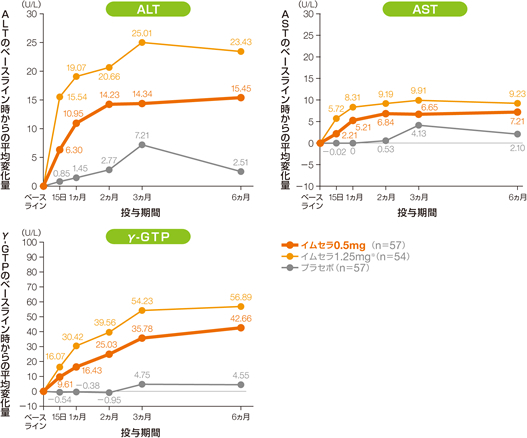
※:本邦におけるイムセラの用法・用量は、1日1回0.5mg
表 肝機能検査値の基準に合致した後に投与中止・中断した症例〔国内第Ⅱ相試験〕
国内臨床試験における肝機能検査値異常の中止・中断基準
| イムセラ | プラセボ群 (n=57) |
||
|---|---|---|---|
| 0.5mg群 (n=57) |
1.25mg※群 (n=54) |
||
| 肝機能検査値の基準に合致した後に投与中止 | 0例(0%) | 2例(3.7%) | 1例(1.8%) |
| ALTがULNの5 倍以上増加 | 0例(0%) | 1例(1.9%) | 1例(1.8%) |
| ASTがULNの5 倍以上増加 | 0例(0%) | 0例(0%) | 0例(0%) |
| 総ビリルビンが2.0mg/dLを超えて増加 | 0例(0%) | 1例(1.9%) | 0例(0%) |
| 投与中断→再開後に投与中止 | 2例(3.5%) | 1例(1.9%) | 0例(0%) |
| 投与再開後、ALTが再度ULNの3倍以上増加 | 2例(3.5%) | 1例(1.9%) | 0例(0%) |
| 投与再開後、ASTが再度ULNの3倍以上増加 | 0例(0%) | 0例(0%) | 0例(0%) |
| 投与中断→再開(投与中止なし) | 1例(1.8%) | 2例(3.7%) | 0例(0%) |
| ALTがULNの3倍以上増加 | 1例(1.8%) | 2例(3.7%) | 0例(0%) 0例 |
| ASTがULNの3倍以上増加 | 0例(0%) | 0例(0%) | (0%) |
ULN:基準値上限
[社内資料]
【肝機能検査値異常の判定基準】
ALT>90U/L、AST>82U/L、γ-GTP>130U/L、総ビリルビン≧2.0mg/dL
(注)国内臨床試験において、肝機能検査値の基準に合致した後、治験薬の投与を1ヵ月以内に中止、または中断した症例の割合を提示した。なお、中止理由、中断理由にかかわらず集計した。
国内第Ⅱ相試験
- 【対象】
- 日本人再発性多発性硬化症患者168例(年齢:18~60歳、EDSS:0~6.0、過去1年間に1回以上または過去2年間に2回以上の再発を経験またはスクリーニング期のGd造影T1強調病巣が1つ以上、試験薬割り付け前30日間に再発を経験していない、スクリーニング期のT2病巣が1つ以上)
- 【方法】
- プラセボ対照・無作為化・二重盲検比較試験。対象患者を無作為に3群に割り付け、イムセラ0.5mg、1.25mg※、またはプラセボの1日1回経口投与を6ヵ月間行い、イムセラの有用性をプラセボと比較検討した。
- 【肝機能異常に関する除外基準】
-
肝臓の状態が以下のいずれかに該当する患者(本試験には肝機能異常のリスクを有する患者は含まれていない)
アルコール乱用や慢性の肝または胆道疾患の既往または合併がある、ASTまたはALTがULN(基準値上限)の2倍を超える、ALPがULNの1.5倍を超える、γ-GTPがULNの3倍を超える、総ビリルビンがULNを超える(ジルベール症候群を除く)、直接ビリルビンがULNを超える
※:本邦におけるイムセラの用法・用量は、1日1回0.5mg
[社内資料]
- リスクを軽減するための注意事項
-
- 肝機能検査の実施について
-
- 肝機能異常が現れることがあるので、イムセラ投与開始前に肝機能検査(トランスアミナーゼ、ビリルビン等)を実施するとともに、本剤投与中は定期的(投与開始15日後、1、2、3、6ヵ月後、それ以降は3ヵ月ごと等)*に肝機能検査を実施してください。
- 本剤投与中に肝機能障害を疑う臨床症状(悪心、嘔吐、腹痛、疲労、食欲不振等)が現れた場合にも肝機能検査を実施し、異常が認められた場合には本剤の投与を中断し、適切な処置を行ってください。
-
- 【慎重投与】について
- 肝機能障害またはその既往歴のある患者に対しては、慎重に投与してください。
*:〔参考〕国内第Ⅱ相試験(6ヵ月)のプロトコールより
